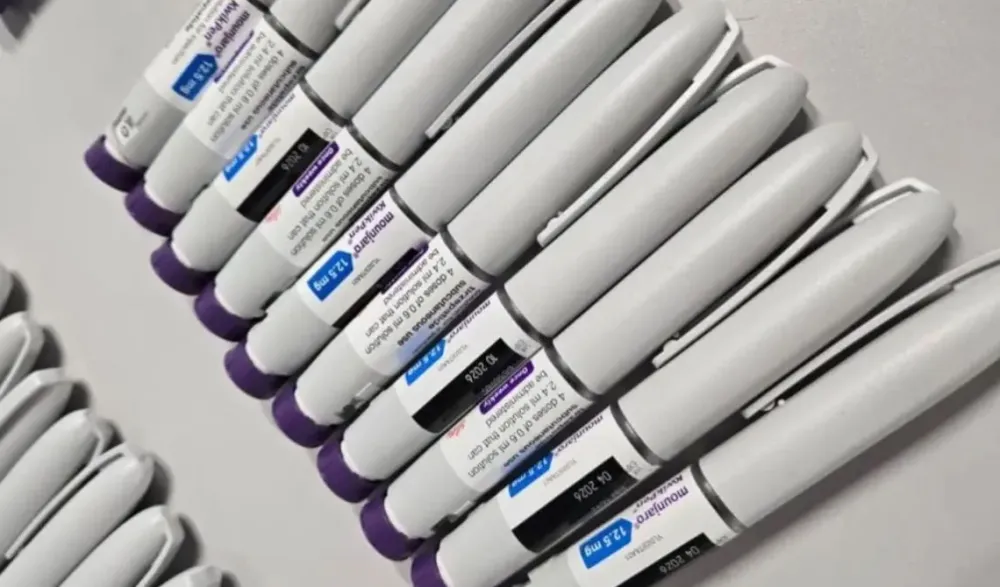
A Anvisa confirmou nesta quinta-feira (21) que diversas canetas emagrecedoras — formuladas com agonistas da GLP-1 e classificadas como medicamentos sem registro — continuam proibidas de serem produzidas, vendidas ou importadas no Brasil, devido à ausência de avaliação oficial de qualidade, eficácia e segurança.
De acordo com a agência, três novas resoluções publicadas nesta semana ampliaram a proibição para fabricação, comercialização, distribuição, importação, transporte e propaganda dos produtos Lipoless Eticos, Tirzazep Royal Pharmaceuticals e T.G. Indufar.
Antes disso, entre setembro e outubro, já haviam sido vetados o Lipoless e o T.G.5 — este último anunciado como tirzepatida, mesma substância presente no Mounjaro.
Em carta pública, a Eli Lilly, responsável pelo Mounjaro, reforçou que é “a detentora exclusiva do único medicamento à base de tirzepatida aprovado pela Anvisa e é a única empresa autorizada a produzir legalmente em larga escala medicamentos contendo este princípio ativo na formulação”.
Segundo a Anvisa, o avanço da propaganda e da comercialização irregular desses produtos, especialmente na internet, motivou a adoção das novas medidas.
“Dessa forma, as medidas foram editadas com o propósito de coibir o desvio de uso desses produtos, a fim de proteger a saúde da população”, afirma o órgão.
A legislação brasileira permite importação de medicamentos sem registro apenas em situações excepcionais, para uso pessoal e com prescrição médica. Entretanto, quando há proibição específica publicada pela Anvisa, a importação, em qualquer formato, também é suspensa. Assim, estão vetados: T.G.5, Lipoless, Lipoless Eticos, Tirzazep Royal Pharmaceuticals e T.G. Indufar.
A Anvisa alerta que produtos sem aprovação no Brasil dificultam a rastreabilidade em caso de eventos adversos e impedem que medidas regulatórias sejam aplicadas se necessário.
Além disso, nenhum medicamento pode ser comercializado com bula apenas em idioma estrangeiro, o que aumenta o risco de falhas de entendimento e erros de administração.
A agência reconhece que, apesar da fiscalização, podem ocorrer casos de falsificação ou adulteração, especialmente quando o produto é fabricado em outros países, fora da regulação brasileira.
Entre os agonistas da GLP-1 autorizados no País, apenas o detentor do registro pode comercializar o produto e é responsável por sua disponibilidade e por eventuais intercorrências.
No Brasil, medicamentos dessa classe só podem ser vendidos mediante prescrição médica com retenção da receita.